Барлық заттар бөлiнбейтiн аса ұсақ бөлшектерден – атомдардан тұрады деген ұғым ерте қалыптасқан болатын. Егер атом шындығында заттың бөлiнбейтiн алғашқы кiрпiштерi болса табиғаттағы кездесетiн сан алуан заттарға сан алуан атомдар сәйкес қойылуы тиiс. Бұлай болуы бiр жағынан күмән туғызады. Физика ғылымының дамуы барысында ХIХ ғасырдың аяғына қарата атомның қасиеттерiне байланысты жаңа тәжiрибелiк деректер жинала бастады. М. Фарадей 1833 жылы электролиз құбылысын зерттеу барысында электролит ертiндiлерiндегi ток иондардың реттелген қозғалысы екенiн анықтады. Ал 1897 жылы Дж. Томсон сиретiлген газдардағы электр разрядын зерттеу барысында қыздырылған немесе ультракүлгiн жарықпен сәулелендiрiлген кез-келген химиялық элементтiң атомы өзiнен терiс зарядталған бөлшектердi шығаратынын анықтады. Осылай алғашқы элементар бөлшек – электрон ашылды. Атом құрлысының күрделiлiгiне нұсқайтын тағы бiр бұлтартпас факт 1869 жылы орыс ғалымы Д.И. Менделеев ашқан химиядық элементтердiң периодтылық заңы. Атомдық масса өскен кезде элементтердiң қасиеттерiнiң қайталануын атомның құрамына кiретiн бөлшектердiң саны өскен кезде оның iшкi құрылымының қандай да бiр ерекшелiгiнiң қайталануымен түсiндiруге болатындай.
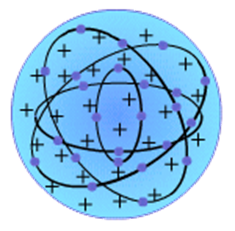
Атомды күрделi жүйе деп ұйғарып, оның алғашқы моделiн ұсынған ғалым – Дж.Томсон. Томсон моделi бойынша атом дегенiмiз радиусы шамамен 10 -10 м болатын шар. Бұл шардың бүкiл көлемi оң зарядталған, ал терiс зарядталған электрондар оның iшiнде су тамшысының iшiнде жүзiп жүрген түйiршiктер тәрiздi қозғалып жүредi (1 - сурет). Томсон моделi атомның бiрқатар қарапайым қасиеттерiн сәттi түсiндiргенiмен көп жағдайда қиыншылыққа тiрелетiн.

1 – сурет
Осы тұрғыдан атом құпиясына терең iрек үңiлiп, оның жаңа бiр модел iн ұсынған ғалым ағылшын оқымыстысы Э. Резерфорд болатын. Ол өз тәжiрибелерiнде аса шапшаң α-бөлшектер жұқа алтын фольгадан шашыраған кездегi бұрыштық таралуын зерттей келе атомның планетарлық моделi деп аталатын моделiн ұсынды. Резерфордтың бұл моделi бойынша атомдағы оң зарядтар Томсон моделi ндегi дей бүкiл көлемде таралмай, керiсiнше, оның орталығында жинақталады. Оны атом ядросы деп атайды. Ал электрондар болса Күн жүйесi ндегi планеталар тәрiздi ядроны айнала қозғалып жүредi (2 - сурет).
Электрондардың массасы аса аз болғандықтан атомның бүкiлдей дерлiк массасы ядрода шоғырланған. Ядроның өлшемi атомның өлшемi мен салыстырғанда шамамен 10 5 еседей кiшi. Атомның ішінде электр зарядтарының орналасу тәртібін анықтау үшін 1911 ж. Резерфорд өзінің шәкірттері Г. Гейгер және Э. Марсденмен бірге α - бөлшектер шоғын өте жұқа алтын фольгадан өткізіп, бірнеше тәжірибелер жасады. Осы тәжірибеді зерделеу нәтижесінде атомның ядролық, басқаша айтсақ, планетарлық моделі өмірге келді. Тәжірибе барысында өте жұқа (l = 6 · 10 м) алтын фольганы энергиясы 7,68 МэВ жылдам α - бөлшектеуімен атқылаған. Қорғасын контейнердің түбінде орналасқан Po радиоактивті элементтен шыққан α - бөлшектердің жіңішке шоғы алтын фольгадан өткенде шашырайды, яғни алғашқы бағытынан ауытқиды. Ол кезде α - бөлшектердің оң зарядты (2е) гелий иондары екені белгілі болатын. Фольгадан шашыраған α - бөлшектердің қаншасы қандай бұрышқа ауытқығанын есептей отырып, осы ауытқуды тудырған нысана атомдың құрылымы анықталды. Фольганың қалыңдығы өте аз болғандықтан, одан өткенде әрбір α - бөлшек тек 1 атоммен ғана әсерлеседі, яғни 1-ақ рет шашырауға ұшырайды деп есептеуге болады. Шашыраған α - бөлшектер күкіртті цинкпен (ZnS) қапталған экранға келіп соғылады. Күкіртті цинк молекула-ының α - бөлшекпен соқтығысқанда сәуле шығаратын қасиеті бар. Сондықтан экранның α - бөлшек соғылатын жерінде сцинтилляция, яғни өте әлсіз жарқыл байқалады. Тәжірибенің мақсаты берілген уақыт аралығында байқалатын жарқылдардың φ ауытқу бұрышына тәуелділігін анықтау. Тәжірибенің нәтижесінде α - бөлшектерді басым көпшілігі фольгадан өткенде алғашқы бағыттан ауытқымайтыны (φ ≈ 1 - 2) анықталды. Бұл нәтиже, негізінен, Томсон моделіне сүйеніп жасалған есептеумен дәл келді. Бірақ, α - бөлшекдің мардымсыз аз бөлігі 90-тан артық бұрышқа ауытқитыны, яғни олар фольгаға соғылып, кері бағытта ұшатыны таңдандырды. 8 мыңға жуық бөлшекдің тек 1-уі ғана осындай үлкен бұрышқа ауытқиды екен. Мұны Томсон моделі негізінде түсіндіру мүмкін болмады. Тәжірибеде алған нәтижелерді зерделей отырып, Резерфорд өз моделін ұсынды. Ол атомның оң заряды оның ортасында орналасқан, радиусы шамамен 10 м өте аз көлемге жинақталған деген қорытындыға келді. Бұл орталық бөлшекті Резерфорд ядро деп атады. Атомның массасы түгел дерлік ядрода шоғырланған. Ядроны айнала әр түрлі орбитамен электрондар қозғалып жүреді. Ең шеткі электрон орбитасының радиусы атомның радиусына тең, R ≈ 10 м. Бұл үлгі күн жүйесінің құрылымына ұқсайтын болғандықтан, оны атомның планетарлық моделі деп те атайды. Модель бойынша атом көлемінің басым көпшілік бөлігі “бос” болып шығады, ядроның радиусы атомның радиусынан 100 000 есе кіші. Орбиталардағы электрондардың теріс зарядтарының қосындысы ядроның оң зарядына тең, атом электрлік бейтарап.
Атомның ішіндегі бос кеңістік “өте үлкен”. Сондықтан, фольга арқылы өткенде α - бөлшекінің көбі ядроданалыс өтеді де,шашырамайды. Электрондар α - бөлшектен 8 мың еседей жеңіл болғандықтан,оның қозғалыс траекториясын өзгерте алмайды. Тек ядроға тікелей қарсы келіп қалған α - бөлшектер ғана онымен әсерлесіп, кері ұшады. Мұндай бөлшектер саны ядро радиусының атом радиусына қатынасымен анықталады.
Резерфорд өз моделінің және Томсон моделінің негізінде есептеу жұмыстарын жүргізді, олардың нәтижесі Резерфорд үлгісінің дұрыстығын көрсетті. Бірақ классикалық физика тұрғысынан мұндай атомның орнықты болуы мүмкін емес. Зарядталған бөлшек үдемелі қозғалса, міндетті түрде сәулеленуі (электромагниттік толқындар шығаруы) керек. Бұл сәулеленудің жиілігі электронның ядро маңында айналу жиілігіне тең болуы тиіс. Электрон ядроны айнала дөңгелек орбитамен қозғалса, оның центрге тартқыш үдеуі бар. Олай болса, электр сәуле шығара отырып, өз энергиясын азайтуы тиіс. Энергияның (орбиталық жылдамдықтың) азаюы ақыры оған құлап түсуіне әкеп соғады. Бұған бар болғаны 10 с-қа тең уақыт кетеді екен және классикалық теория бойынша мұндай атомның сәулелену спектрі тұтас болу керек, ал шын мәнінде атомдық спектр сызықтық болады.