4.1 Теоретические основы кислотно-основого титрования
Метод кислотно-основного титрования основан на реакциях взаимодействия между кислотами и основаниями, то есть на реакции нейтрализации полуреакция (6):
Н + + ОН - ↔ Н 2 О
Рабочими растворами метода являются растворы сильных кислот (HCl, H2S, НNОз и др.) или сильных оснований (NaOH, КОН, Ва(ОН)2 и др.). В зависимости от титранта метод кислотно-основного титрования подразделяют на ацидиметрию, если титрантом является раствор кислоты, и алкалиметрию, если титрантом является раствор основания.

титрант –кислота титрант- основание
ОН- + Н3О+ →2Н2О Н3О+ + ОН- →2Н2О
Рабочие растворы в основном готовят как вторичные стандартные растворы, поскольку исходные для их приготовления вещества не являются стандaртными, а затем их стандартизуют по стандартным веществам или стандартным растворам. Например: растворы кислот можно стандартизовать по стандартным веществам - натрия тетраборату Na 2 B4О7 ∙10Н 2 О, натрия карбонату Nа 2 СО 3 ∙10Н 2 О или по стандартным растворам NaOH, КОН; а растворы оснований - по щавелевой кислоте Н 2 С 2 О 4 ∙ 2Н 2 О, янтарной кислоте Н 2 С 4 Н 4 О 4 или по стандартным растворам HCl, H 2 SO 4 , НNО 3 .
Точка эквивалентности и конечная точка титрования. Согласно правилу эквивалентности титрование необходимо продолжать до тех пор, пока количество прибавленного реагента не станет эквивалентным содержанию определяемого вещества. Наступающий в процессе титрования момент, когда количecтвo стандартного раствора реагента (титранта) становится теоретически строго эквивалентным количеству определяемого вещества согласно определенному уравнению химической реакции, называют точкой эквивалентности.
Точку эквивалентности устанавливают различными способами, например по изменению окраски индикатора, прибавляемого в титруемый раствор. Момент, при котором происходит наблюдаемое изменение цвета индикатора, называют конечной точкой титрования. Очень часто конечная точка титрования не совсем совпадает с точкой эквивалентности. Как правило, они отличаются друг от друга не более чем на 0,02-0,04 мл (1-2 капли) титранта. Это то количество титранта, которое необходимо для взаимодейcтвия с индикатором.
Измерив объем Vт титранта в конце титрования, рассчитывают концентрацию С анализируемого раствора по закону эквивалентов, которая выражается формулой 18.
CаVа= CтVт (концентрации выражены в моль/л) (18)
Отсюда следует формула 19.
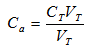 (19)
(19)
Теоретически необходимо добавить такой объем титранта, который содержит количество реагента, эквивалентное количеству определяемого компонента в соответствии со стехиометрией реакции между ними при условии, что эта реакция практически необратима.